5月30日-6月3日,2025年美国临床肿瘤学会(ASCO)年会在美国芝加哥举行。上海细胞治疗集团在会上公布了基于全球自主知识产权JL基因写入系统的自分泌PD1纳米抗体的闪CAR-T细胞药物在(aPD1-MSLN JL-Lightning CAR-T™)晚期恶性间皮瘤患者的I期临床研究的初步数据,验证了自分泌PD-1纳米抗体的闪CAR-T在实体瘤治疗领域的潜在价值,也为未来肿瘤免疫治疗提供新思路。
ASCO年会是全球肿瘤领域最权威的学术交流盛会,每年都会展示当前国际最前沿的临床肿瘤学科研成果和治疗技术。本次年会,上海细胞治疗集团新药创制BG总裁刘颐博士现场参加会议并做了壁报展示。
产品:非病毒载体 aPD1-MSLN JL-Lightning CAR-T细胞
药物靶点+类型:间皮素+免疫检查点抗体装甲化+JL基因写入系统闪CAR-T
研发赛道:全球首个PD1纳米抗体装甲化实体瘤闪CAR-T
本次展示产品搭载集团自主研发的JL-闪CAR-T™技术平台,依托于集团高效低毒JL基因写入技术、体内连续增殖纳米抗体发现技术和T细胞靶向核酸递送系统三大底层技术,仅需30小时(30h)完成从单采血到制剂的全过程,7例回输可评价受试者,总体客观缓解率(ORR)为57%,疾病控制率(DCR)为86%。
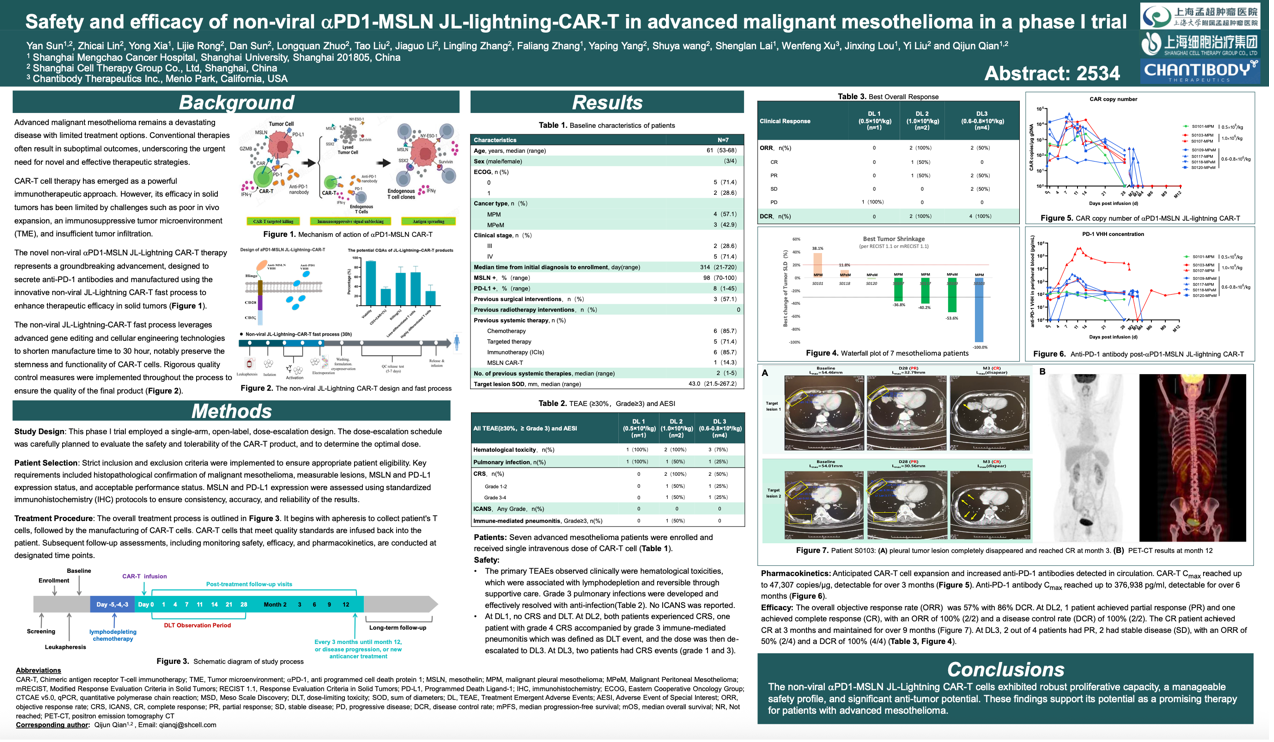
摘要号:2534
摘要题目:
Safety and efficacy of non-viral aPD1-MSLN JL-lightning-CAR-T in advanced malignant mesothelioma in a phase I trial
摘要内容:
恶性间皮瘤是一种侵袭性强的恶性肿瘤,起源于间皮细胞,可见于胸膜、腹膜、心包膜以及睾丸的浆膜,其中胸膜间皮瘤最为常见。其恶性程度高,病变广泛,部分病人进展极快、死亡率高、预后差。目前治疗恶性间皮瘤的手段有限、效果不甚理想,导致恶性间皮瘤患者的中位总生存期(overall survival,OS)仅为1年左右。传统疗法往往效果不佳,凸显了创新方法的迫切需求。CAR-T细胞疗法已成为一种强大的免疫治疗策略,在血液肿瘤治疗上带来治愈性的突破。然而,其在实体瘤中的应用受到体内增殖差、免疫抑制性微环境(TME)和肿瘤浸润不足等挑战。
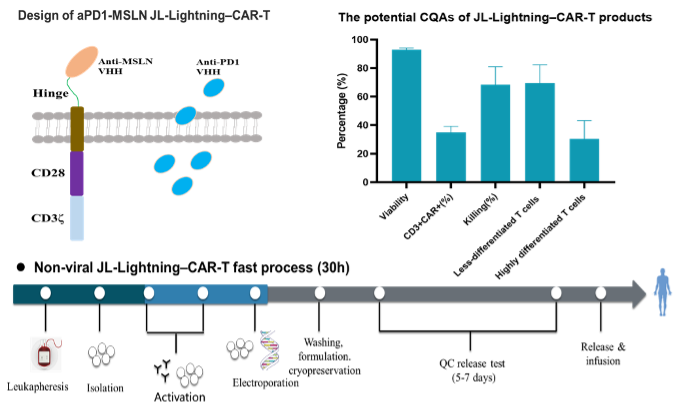
图1. 新型非病毒aPD1-MSLN JL-Lightning-CAR-T
新型非病毒aPD1-MSLN JL-Lightning-CAR-T疗法的开发是MSLN靶向的实体瘤治疗的一项突破性进展。利用CAR-T自分泌PD-1纳米抗体专利技术,通过自主知识产权的JL基因写入系统开发的非病毒JL-Lightning-CAR-T快速工艺将制造时间缩短到30小时,快速制造干性强、增殖潜力高的CAR-T细胞,提升体内的增殖能力。aPD1-MSLN JL-Lightning-CAR-T细胞在体内高水平分泌PD-1纳米抗体,一方面结合CAR-T细胞本身PD1分子,降低CAR-T细胞耗竭,提升体内的持久性;另一方面高亲和力的PD1纳米抗体可以竞争阻断肿瘤组织内环境中PD-1/PD-L1的结合,解除对内源性免疫细胞的抑制,释放内源性免疫细胞的抗肿瘤活性,提升实体瘤的抗肿瘤疗效。非病毒JL-Lightning-CAR-T快速制造的整个生产过程中严格执行质量控制措施,以确保最终产品的高质量。
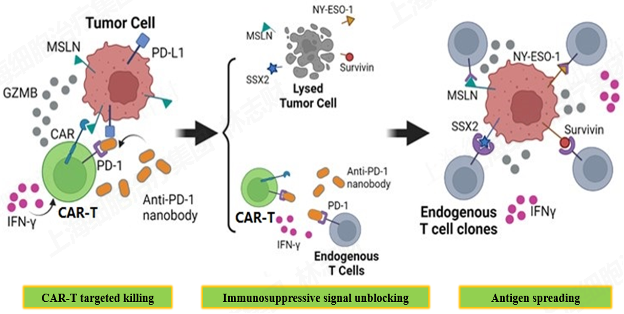
图2. aPD1-MSLN JL-Lightning-CAR-T的作用机制
针对创新型非病毒aPD1-MSLN JL-Lightning-CAR-T产品,设计并开展了本项I期临床试验,采用单臂、开放标签、剂量递增设计,以评估创新CAR-T的安全性、耐受性以及初步疗效。
本研究设定了严格的纳入和排除标准,确保入组受试者符合入组要求。恶性间皮瘤患者诊断需要组织病理学确认,MSLN和PD-L1表达通过IHC检测以确保准确可靠。

图3. aPD1-MSLN JL-Lightning-CAR-T的临床研究流程
整个治疗流程包括采集患者的T细胞,随后进行JL-Lightning-CAR-T 细胞快速制备,最后完成质量放行的CAR-T细胞进行临床回输。按照研究规定的访视时间点进行随访评估,包括安全性、有效性和药代动力学等。
此次ASCO会议报道了最新的研究结果。7例入组的晚期恶性间皮瘤患者,均接受了单次静脉回输。临床观察到的主要治疗相关不良事件(TEAE)为血液学毒性,考虑与清淋预处理相关,通过对症支持快速逆转。研究中发生了3级肺部感染,并通过积极的抗感染治疗得到有效控制。本研究所有患者均未观察到免疫效应细胞相关神经毒性综合征(ICANS)。在第一剂量组(DL1,n=1),未观察到CRS和剂量限制性毒性(DLT)。在第二剂量组(DL2,n=2),2例患者均发生了CRS,1例患者发生4级CRS,伴有3级免疫介导性肺炎,定义为DLT事件,经安全委员会评估决议剂量降至第三剂量组(DL3,n=4)。在第三剂量组(DL3,n=4),其中2例患者发生CRS(分别为1级与3级)。CAR-T细胞回输后,外周循环中能检测到高水平的CAR-T增殖和PD-1纳米抗体分泌。CAR-T Cmax值最高达到47307 copies/µg,持续超过3个月可检测到。PD-1纳米抗体Cmax值最高达376938 pg/ml,持续超过6个月可有效检出。
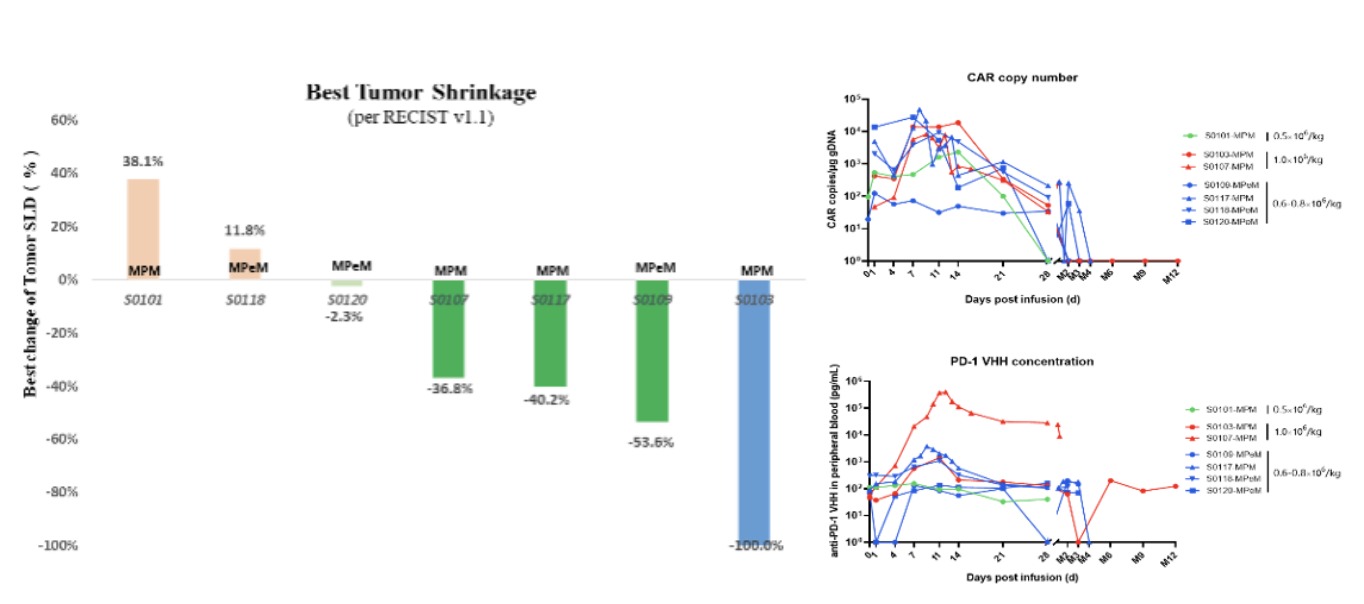 图4. aPD1-MSLN JL-Lightning-CAR-T体内增殖显著且抗肿瘤疗效突出
图4. aPD1-MSLN JL-Lightning-CAR-T体内增殖显著且抗肿瘤疗效突出
7例回输可评价受试者,总体客观缓解率(ORR)为57%,疾病控制率(DCR)为86%。在第二剂量组(DL2,n=2),1例患者达到部分缓解(PR),1例患者实现完全缓解(CR),ORR与DCR均为100%(2/2)。其中,CR患者在3个月时获得肿瘤完全缓解,持续CR已超过12个月。在第三剂量组(DL3,n=4),4例患者中有2例达到PR,2例为疾病稳定(SD),ORR为50%(2/4),DCR为100%(4/4)。
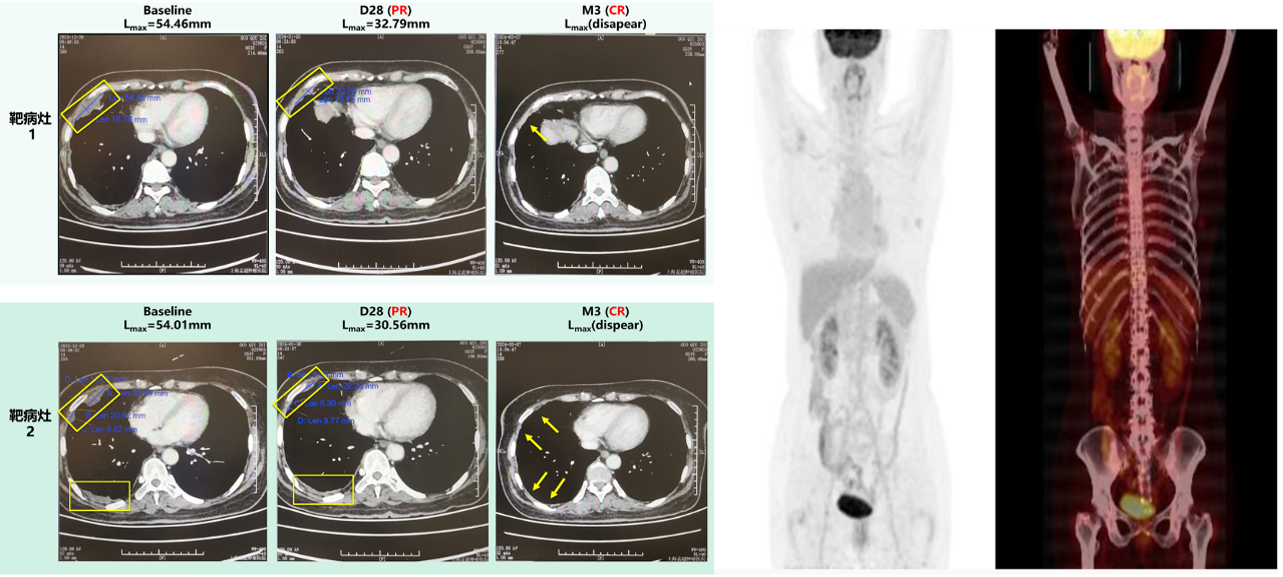 图5. aPD1-MSLN JL-Lightning-CAR-T 实现恶性间皮瘤完全缓解(CR)
图5. aPD1-MSLN JL-Lightning-CAR-T 实现恶性间皮瘤完全缓解(CR)
结论:初步临床研究结果显示JL-闪CAR-T™平台工艺制备的非病毒aPD1-MSLN JL-Lightning-CAR-T细胞,具备高活性低分化的产品品质特征,表现出优异的体内药代动力学扩增能力(PK),可控的安全性以及突出的抗肿瘤疗效(总体ORR=57%)。基于全球自主知识产权JL基因写入系统的aPD1-MSLN JL-Lightning-CAR-T产品极具潜力,或成为晚期间皮瘤或其他间皮素阳性肿瘤的一种有前景的治疗方法。
