4月25日-30日,备受关注的美国癌症研究协会(AACR)年会在美国芝加哥召开,本届会议以“统一癌症科学与医学:持续创新带来变革”为主题。秉持“疗效为核,百姓可及”的药物开发理念,上海细胞治疗集团持续推动JL-闪CAR-T™为核心的关键技术平台开发,实现原创非病毒载体基因写入技术、纳米抗体VHHMAb®技术等底层技术的持续突破,加速创新治疗药物开发进程。本次会议,集团共有5项最新研究成果获邀现场展示,覆盖从底层平台突破到优势抗体发现,再到临床应用转化的完整药物开发体系。充分展现了集团在革新CAR-T等创新细胞药物可及性和治愈性方面的前瞻布局及广阔前景。

BZE2203为一项治疗实体肿瘤的自分泌抗PD-1纳米抗体装甲化双靶向MUC1和MSLN的CAR-T细胞治疗项目。由上海细胞治疗集团联合上海大学附属孟超肿瘤医院及美国子公司Chantibody(CHANTIBODY THERAPEUTICS INC.)共同开展。
BZE2203采用条件激活型CAR结构设计,依托于集团第四代纳米抗体VHHMAb®技术平台开发的肿瘤特异性结合MUC1纳米抗体、pH依赖的MSLN纳米抗体和高亲和力分泌型的PD-1纳米抗体,结合自主创新的基因写入系统和JL-闪CAR-T™技术平台开发的免疫检查点抗体装甲化双靶向的实体瘤闪CAR-T。具备低分化、体内增殖持续性好、自分泌抗PD-1纳米抗体等特性,以减轻TME对CAR-T细胞和肿瘤浸润淋巴细胞的抑制作用。目前开展的IIT临床实验中,首次入组的两例铂类耐药卵巢癌患者,接受了5×105CAR-T/kg低剂量CAR-T细胞回输, 临床观察安全性良好,无DLT,未观察到CRS、ICANS等副作用。两例患者回输后均获得部分缓解(PR),1例持续缓解至M3肿瘤靶病灶消失,达到完全缓解(CR),临床疗效显著。

摘要号:4799
摘要题目:
MSLN and MUC1 dual-targeting CAR-T with conditional activation and tumor specificity to improve clinical safety and efficacy
摘要内容:
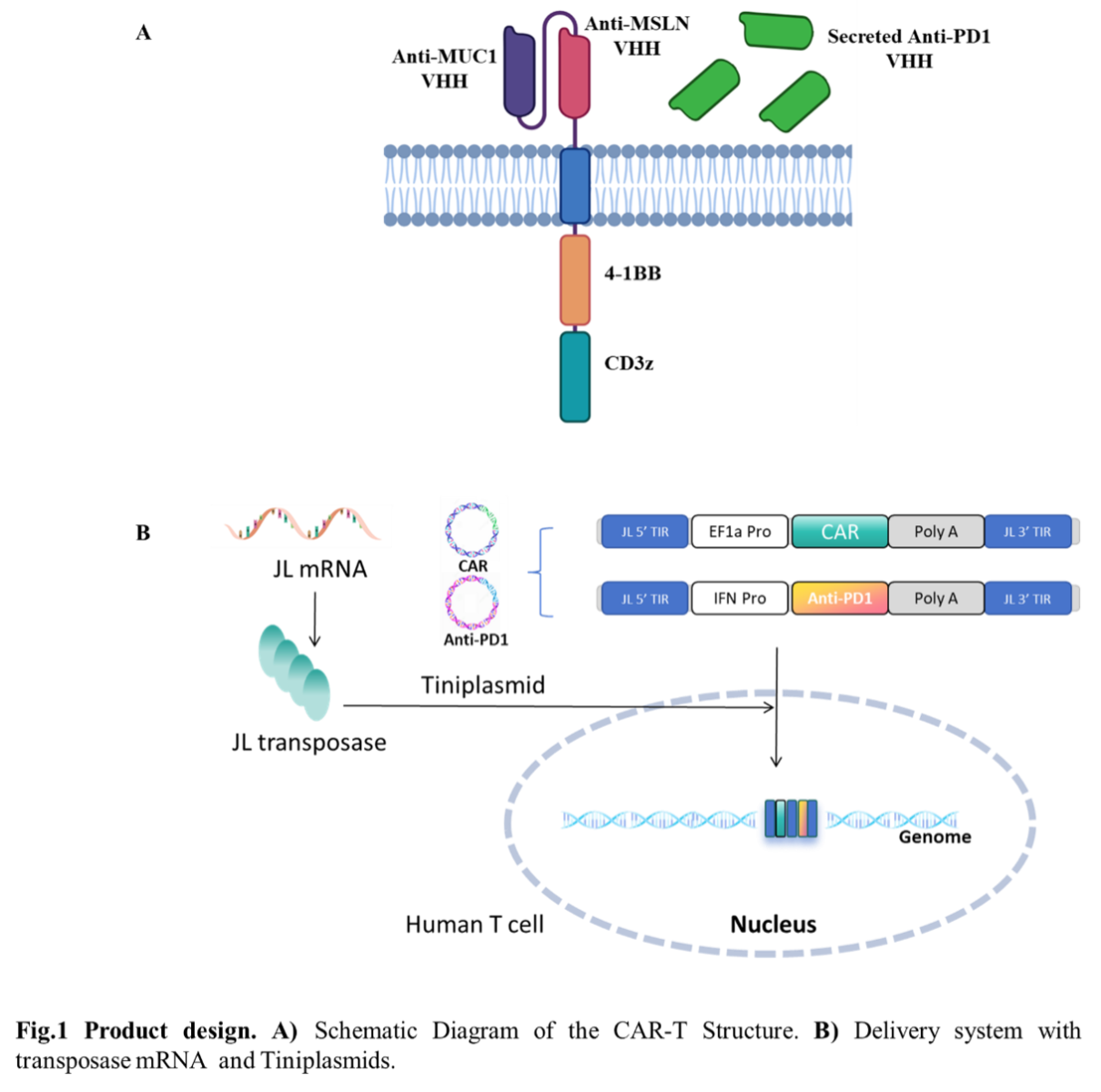
MSLN(间皮素)和MUC1(黏蛋白1)在许多实体瘤中高表达,使其成为实体瘤靶向治疗的潜在靶点。然而,这两个靶点在重要的人体组织中也显示出不同程度的表达,在CAR-T疗法中可能引发“靶向非肿瘤”效应的风险。此外,肿瘤免疫微环境(TME)对CAR-T细胞具有强烈的免疫抑制作用,使其易于衰竭,从而难以发挥持久的抗肿瘤效应。我们构建了一种MSLN/MUC1双靶向CAR-T,同时,该CAR-T可以分泌抗PD-1纳米抗体以减轻TME对CAR-T细胞和肿瘤浸润淋巴细胞的抑制作用(图1)。
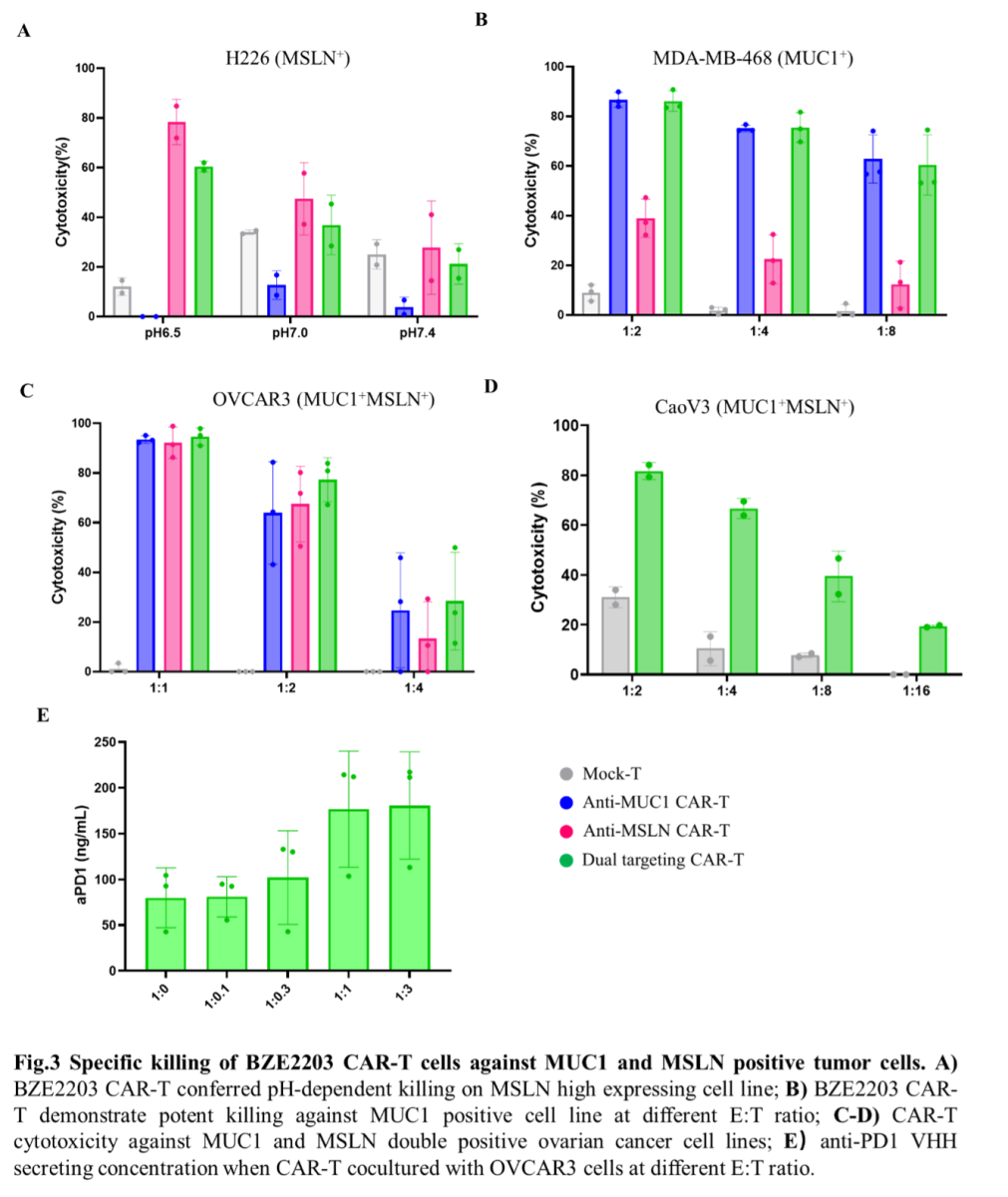
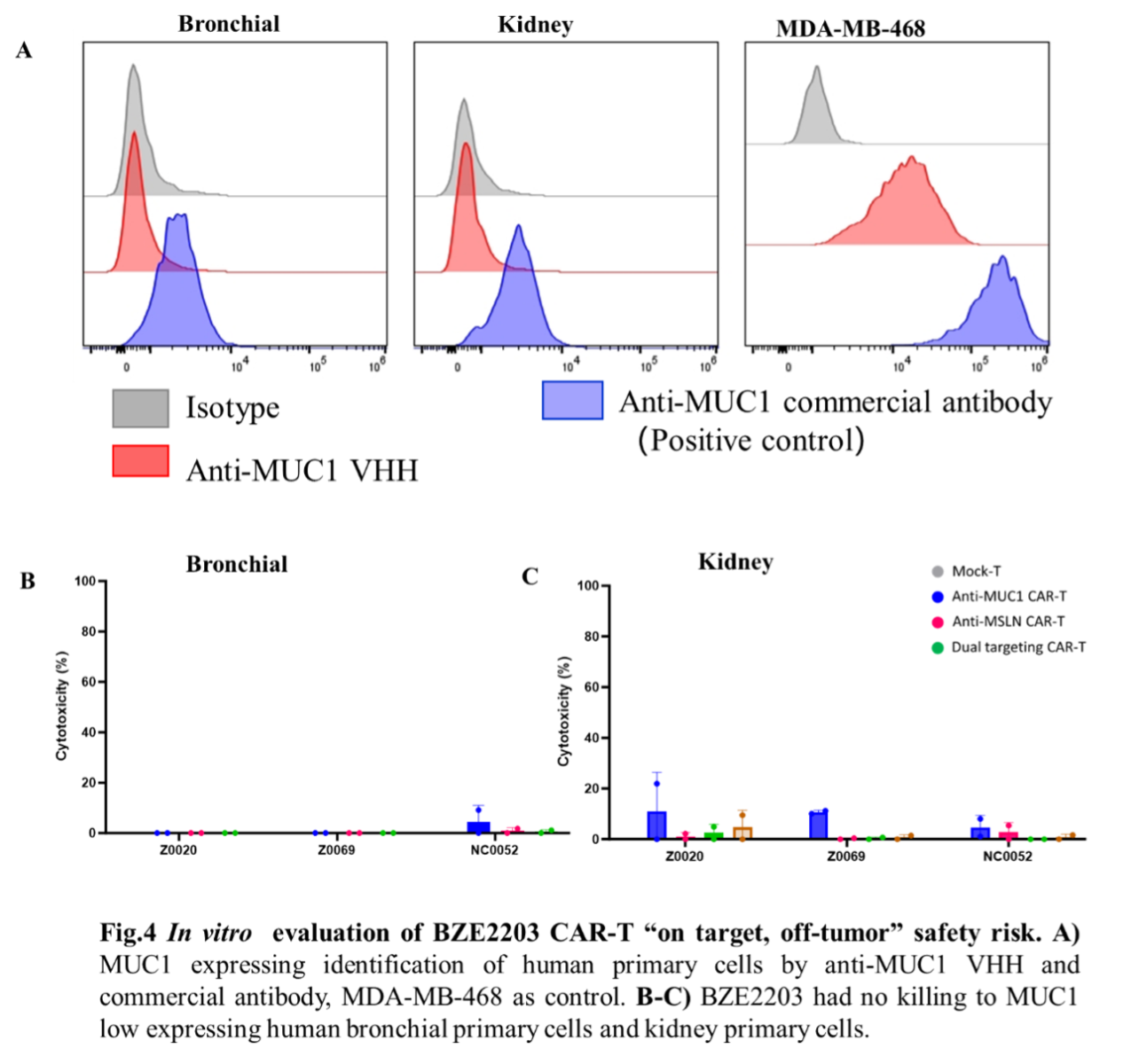
抗MSLN的VHH通过工程设计赋予其pH依赖性结合特征,使CAR-T细胞仅在TME中的酸性环境下具有对靶细胞的杀伤功能(图3A)。抗MUC1的VHH则根据抗原密度依赖性进行设计,以确保其可以高效杀伤肿瘤细胞(图3B-D),但对低MUC1表达的正常组织原代细胞无细胞毒性(图4)。
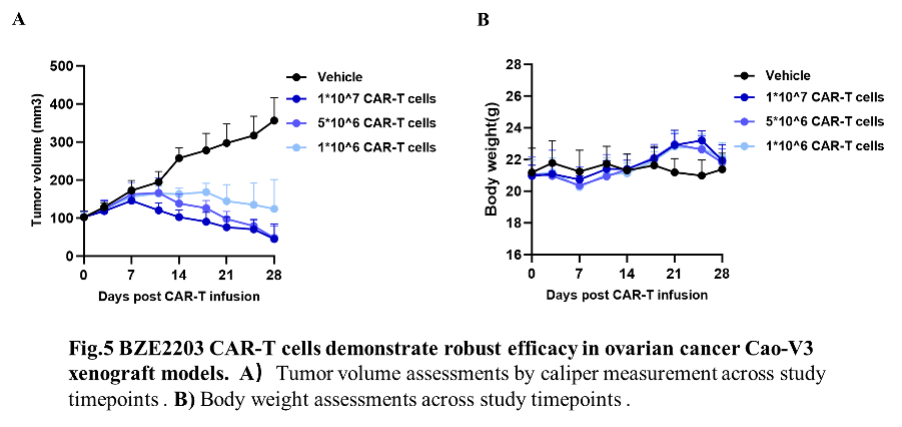
在完成体外概念验证后,我们使用Cao-V3异种移植肿瘤模型来评估BZE2203 CAR-T的体内安全性和有效性。在不同剂量CAR-T回输下,均呈现出对肿瘤的高效清除功能,并且在高剂量下(1×107 CAR-T cells)显示具有良好的体内耐受性(图5)。
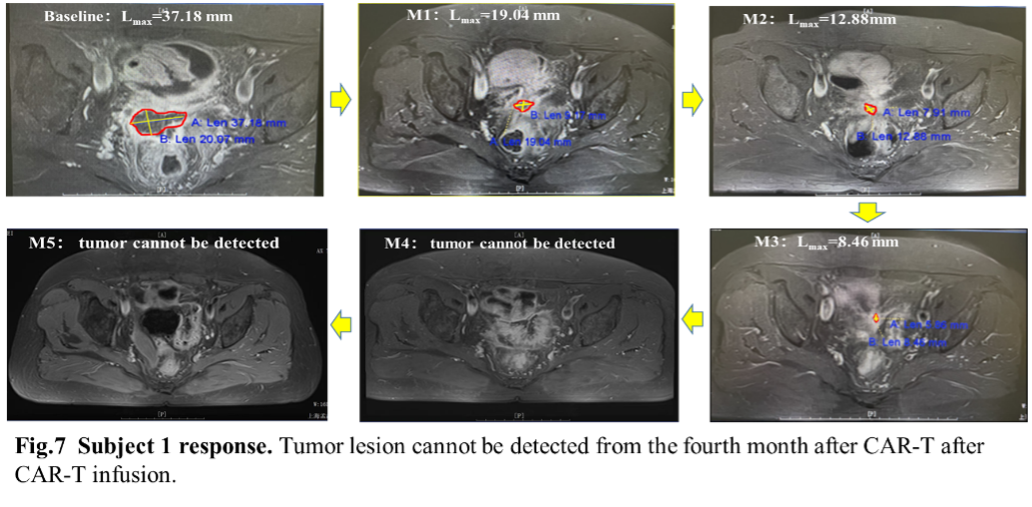
在完成临床前验证后,我们启动了一项针对复发性卵巢恶性肿瘤的IIT临床试验(NCT06327997),第一剂量组招募了两名铂类耐药的卵巢癌晚期患者,并通过低剂量BZE2203 CAR-T细胞(5×105 CAR-T cells/Kg)的回输来初步评估该产品的安全性和有效性。两例患者均未出现任何CAR-T相关的CRS、ICANS和脱靶毒性等安全性问题;两例患者回输后均在首月获得部分缓解(PR),1例持续缓解至M3肿瘤靶病灶消失,达到完全缓解(CR),临床疗效显著(图7)。

结论:
1. 靶向MUC1和MSLN的双特异性纳米抗体在MUC1靶点阳性的肿瘤细胞系上表现出良好的结合,但与低表达MUC1的原代细胞上无结合;在pH 7.4条件下,对MSLN无结合能力。
2. BZE2203 CAR-T在体外和体内实验中表现出了对肿瘤细胞强劲的杀伤能力,并且对靶点阳性的人原代细胞没有杀伤能力。条件型激活的CAR-T设计有效解决了“on-target, off tumor”毒性问题。
3. 在IIT临床试验中,首次入组的前2名铂耐药卵巢癌患者在CAR-T细胞输注后达到部分缓解,且未观察到CAR-T引起的安全性问题,支持该CAR-T做更高剂量的临床研究。
